Bài 32.5 Trang 41 Sách bài tập (SBT) Hóa học 9
32.5. Có 4 lá kim loại: sắt, đồng, nhôm, bạc. Làm thế nào để có thể nhận biết được mỗi kim loại bằng phương pháp hoá học. Viết các phương trình hoá học.
Trả lời
- Kim loại nào tan trong dung dịch NaOH đặc tạo bọt khí bay ra là Al.
\(2Al + 2NaOH + 2{H_2}O \to 2NaAl{O_2} + 3{H_2} \uparrow \)
- Ba kim loại còn lại, kim loại nào tan trong dung dịch HCl và tạo bọt khí bay lên là Fe.
\(Fe + 2HCl \to FeC{l_2} + {H_2} \uparrow \)
- Hai kim loại còn lại, kim loại nào đẩy được bạc ra khỏi dung dịch AgNO3 là Cu.
\(Cu + 2AgN{O_3} \to Cu{(N{O_3})_2} + 2Ag \downarrow \)
- Kim loại còn lại là Ag (không phản ứng với dung dịch AgN03).
Bài 32.6 Trang 41 Sách bài tập (SBT) Hóa học 9
32.6. Trong phòng thí nghiệm có 3 lọ mất nhãn đựng ba chất bột trắng là : BaC03, NaCl, Na2C03. Làm thế nào để nhận ra hoá chất trong mỗi lọ với điều kiện chỉ dùng thêm dung dịch HCl loãng ?
Trả lời
- Lần lượt cho 3 chất vào 3 ống nghiệm đựng dung dịch HCl, nếu chất nào tan và có khí bay ra là Na2C03, BaC03 và chất nào tan mà không có khí bay ra là NaCl.
Na2C03 + 2HCl —> 2NaCl + C02 + H20 (1)
BaCO3 + 2HCl —> BaCl2 + C02 + H20 (2)
- Sau đó hoà tan một ít Na2C03 và BaC03 vào nước. Chất nào tan trong nước là Na2C03
Chất không tan trong nước là BaC03.
Bài 32.7 Trang 41 Sách bài tập (SBT) Hóa học 9
32.7. Hình vẽ 3.5 là thiết bị điều chế khí clo trong phòng thí nghiệm.
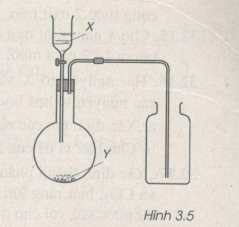
a) X và Y là những chất nào trong số các chất sau ?
X : H2O, dd HCl, dd H2SO4, dd NaOH, dd NaCl.
Y : NaCl, CaCO3, MnO2, CuCl2, Na2S04, KMn04.
Viết phương trình hoá học điều chế khí clo từ những chất đã chọn ở trên.
Trả lời
a) X là : dd HC
Y là : MnO2, KMnO4
b) Phương trình hoá học của phản ứng điều chế clo.
\(Mn{O_2} + 4HCl \to MnC{l_2} + 2{H_2}O + C{l_2} \uparrow \)
\(2KMn{O_4} + 16HCl \to 2KCl + 2MnC{l_2} + 5C{l_2} \uparrow + 8{H_2}O\)
Bài 32.8 Trang 41 Sách bài tập (SBT) Hóa học 9
32.8. Một nguyên tố X tạo được các hợp chất sau : XH3, X205. Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tố X cùng nhóm với
A. agon ; B. nitơ ;
C. oxi ; D. flo.
Trả lời
Đáp án B.
Giaibaitap.me
Giải bài tập trang 41 bài 32 ôn tập chương 3 Sách bài tập (SBT) Hóa học 9. Câu 32.9: Cho kim loại Al có dư vào 400 ml dung dịch HCl 1M. Dẫn khí tạo ra qua ống đựng CuO dư....
Giải bài tập trang 42 bài 32 ôn tập chương 3 Sách bài tập (SBT) Hóa học 9. Câu 32.13: Cho 23,6 gam hỗn hợp gồm Mg, Fe, Cu tác dụng vừa hết với 91,25 gam dung dịch HCl 20% thu được...
Giải bài tập Trang 42 bài 32 ôn tập chương 3 Sách bài tập (SBT) Hóa học 9. Câu 32.16: Hai nguyên tố X và Y ở hai chu kì kế tiếp nhau trong bảng tuần hoàn các nguyên tố hoá học và có tổng số điện tích hạt nhân là 16...
Giải bài tập trang 42 bài 32 ôn tập chương 3 Sách bài tập (SBT) Hóa học 9. Câu 32.20: X, Y là hai nguyên tố halogen thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Hỗn hợp A chứa 2 muối X, Y với natri...
