Bài 1 trang 82 sgk hoá học 10
Cho các phản ứng sau :
A. 2HgO \( \xrightarrow[]{t^{0}}\) 2Hg + O2
B. СаСОз \( \xrightarrow[]{t^{0}}\) CaO + CO2.
C. 2Al(OH)3 \( \xrightarrow[]{t^{0}}\) Al2O3 + 3H2O
D. 2NaHCO3 \( \xrightarrow[]{t^{0}}\) Na2CO3 + CO2 + H2O
Phản ứng nào là phản ứng oxi hoá - khử.
Lời giải:
Chọn A
Bài 2 trang 82 sgk hoá học 10
Cho các phản ứng sau :
A. 4NH3 + 5O2 —> 4NO + 6H2O
B. 2NH3 + 3Cl2 —> N2 + 6HCl
C. NH3 + 3CuO —> 3Cu + N2 + 3H2O
D. 2NH3 + H2O2 + MnS04 —> Mn02 + (NH4)2SO4.
Ở phản ứng nào NH3 không đóng vai trò chất khử ?
Lời giải:
Chọn D
Bài 3 trang 83 sgk hoá học 10
Trong số các phản ứng sau :
A. HNO3 + NaOH → NaNO3 + H2O
B. N2O5+ H2O → 2HNO3
C. 2HNO3 + 3H2S → 3S + 2NO + 4H2O
D. 2Fe(OH)3 → Fe2O3 + 3H2O.
Phản ứng nào là phản ứng oxi hoá - khử.
LỜI GIẢI
Trong các phản ứng trên chi có phản ứng C là phản ứng oxi hoá - khử vì có sự thay đổi số oxi hoá của các nguyên tố.
Bài 4 trang 83 sgk hoá học 10
Trong phản ứng : 3NO2 + H2O → 2HNO3 + NO
NO2 đóng vai trò gì ?
A. Chỉ là chất oxí hoá.
B. Chỉ là chất khử.
C. Là chất oxi hoá, nhưng đồng thời cũng là chất khử.
D. Không là chất oxi hoá, không là chất khử.
Chọn đáp án đúng.
LỜI GIẢI
NO2 đóng vai trò vừa là chất oxi hoá vừa là chất khử : C đúng.
Bài 5 trang 83 sgk hoá học 10
Phân biệt chất oxi hoá và sự oxi hoá, chất khử và sự khử. Lấy thí dụ để minh họa.
LỜI GIẢI
Chất oxi hoá là chất nhận electron.
Sự oxi hoá một chất là làm cho chất đó nhường electron.
Chất khử là chất nhường electron.
Sự khử một chất là sự làm cho chất đó thu electron.
Thí dụ: Fe + CuSO4 → FeSO4 + Cu
- Nguyên tử Fe nhường elcctron, là chất khử. Sự nhường electron của Fe được gọi là sự oxi hoá nguyên tử sắt.
- Ion đồng nhận electron, là chất oxi hoá. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Bài 6 trang 83 sgk hoá học 10
Thế nào là phản ứng oxi hoá - khử ? Lấy ba thí dụ.
LỜI GIẢI
Phản ứng oxi hoá - khử là phản ứng hoá học trong đó có sự chuyển electron giữa các chất phản ứng.
Thí dụ:
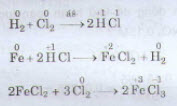
Bài 7 trang 83 sgk hoá học 10
Lập phương trình phản ứng oxi hoá - khử sau đây theo phương pháp thăng bằng electron :
a) Cho MnO2 tác dụng với dung dịch axit HCl đặc, thu được MnCl2, Cl2 và H2O.
b) Cho Cu tác dụng với dung dịch axit HNO3 đặc, nóng thu được Cu(NO3)2, NO2 và H2O.
c) Cho Mg tác dụng với dung dịch axit H2SO4 đặc, nóng thu được MgSO4, s và H2O.
Lời giải
Các phương trình phán ứng oxi hoá - khử :
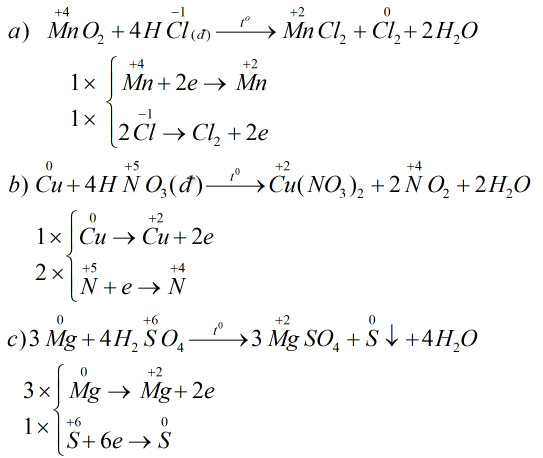
Bài 8 trang 83 sgk hoá học 10
Cần bao nhiêu gam đồng để khử hoàn toàn lượng ion bạc có trong 85 ml dung dịch AgNO3 0,15M ?
LỜI GIẢI
\( n_{AgNO_{3}}\) = \( \frac{0,15.85}{1000}\) = 0,01275 mol
Phương trình hoá học của phản ứng :
Cu + 2AgNO3 -> Cu(NO3)2 + 2Ag
1mol 2mol
x mol ← 0,01275 mol
x = \( \frac{0,01275}{2}\) = 0,006375 mol
mCu tham gia phản ứng : 0,006375 X 64 = 0,408 g.
Giaibaitap.me
Giải bài tập trang 86, 87 bài 18 Phân loại phản ứng trong hóa học vô cơ Sách giáo khoa (SGK) Hóa học 10. Câu 1: Trong phản ứng này, nguyên tử natri...
Giải bài tập trang 86, 87 bài 18 Phân loại phản ứng trong hóa học vô cơ Sách giáo khoa (SGK) Hóa học 10. Câu 6: Lấy ba thí dụ phản ứng hoá hợp thuộc loại phản ứng oxi hoá ...
Giải bài tập trang 88, 89 bài 19 Luyện tập: Phản ứng oxi hóa - khử Sách giáo khoa (SGK) Hóa học 10. Câu 1: Loại phản ứng nào sau đây luôn luôn không là loại phản ứng oxi hoá - khử...
Giải bài tập trang 88, 89 bài 19 Luyện tập: Phản ứng oxi hóa - khử Sách giáo khoa (SGK) Hóa học 10. Câu 7: Dựa vào sự thay đổi số oxi hoá, tìm chất oxi hoá và chất khử trong những phản ứng sau ...
