Bài 1 trang 75 SGK Hóa học 10 Nâng cao
Chọn định nghĩa đúng nhất về liên kết cộng hóa trị.
Liên kết cộng hóa trị là liên kết
A. giữa các phi kim với nhau.
B. trong đó cặp electron chung bị lệch về một nguyên tử.
C. được hình thành do sự dùng chung electron của 2 nguyên tử khác nhau.
D. được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron chung.
Giải
Chọn D.
Bài 2 trang 75 SGK Hóa học 10 Nâng cao
tử \(C{H_4}\) , giữa nguyên tử O và các nguyên tử H trong phân tử \({H_2}O\), giữa nguyên tử S và các nguyên tử H trong phân tử \({H_2}S\).
Giải
- Trong phân tử \(C{H_4}\), nguyên tử cacbon bỏ ra 4 electron lớp ngoài cùng tạo thành 4 cặp electron chung với 4 nguyên tử hiđro. Mỗi nguyên tử trong phân tử \(C{H_4}\) đều đạt được cấu hình bền vững của nguyên tử khí hiếm gần nhất: Mỗi nguyên tử hiđro có 2 electron (giống He), còn nguyên tử cacbon có 8 electron lớp ngoài cùng (giống Ne).
- Trong phân tử \({H_2}O\), nguyên tử oxi bỏ ra 2 electron lớp ngoài cùng tạo thành 2 cặp electron chung với 2 nguyên tử hiđro. Mỗi nguyên tử trong phân tử \({H_2}O\) đều đạt được cấu hình bền vững của nguyên tử khí hiếm gần nhất: Mỗi nguyên tử hiđro có 2 electron (giống He), còn nguyên tử oxi có 8 electron lớp ngoài cùng (giống Ne).
- Trong phân tử \({H_2}S\), nguyên tử lưu huỳnh bỏ ra 2 electron lớp ngoài cùng tạo thành 2 cặp electron chung với 2 nguyên tử hiđro. Mỗi nguyên tử trong phân tử \({H_2}S\) đều đạt được cấu hình bền vững của nguyên tử khí hiếm gần nhất: Mỗi nguyên tử hiđro có 2 electron (giống He), còn nguyên tử lưu huỳnh có 8 electron lớp ngoài cùng.
Bài 3 trang 75 SGK Hóa học 10 Nâng cao
Giải thích sự hình thành cặp electron liên kết giữa hai nguyên tử N trong phân tử \({N_2}\), giữa nguyên tử H và nguyên tử Cl trong phân tử HCl.
Giải
- Trong phân tử \({N_2}\) , mỗi nguyên tử nitơ bỏ ra 3 electron lớp ngoài cùng tạo thành 3 cặp electron chung giữa hai nguyên tử nitơ. Mỗi nguyên tử trong phân tử \({N_2}\) đều đạt được cấu hình bền vững của nguyên tử khí hiếm gần nhất: Mỗi nguyên tử nitơ có 8 electron lớp ngoài cùng.
- Trong phân tử HCl, nguyên tử clo bỏ ra 1 electron lớp ngoài cùng tạo thành 1 cặp electron chung với 1 nguyên tử hiđro. Mỗi nguyên tử trong phân tử HCl đều đạt được cấu hình bền vững của nguyên tử khí hiếm gần nhất: Mỗi nguyên tử hiđro có 2 electron (giống He), còn nguyên tử clo có 8 electron lớp ngoài cùng.
Bài 4 trang 75 SGK Hóa học 10 Nâng cao
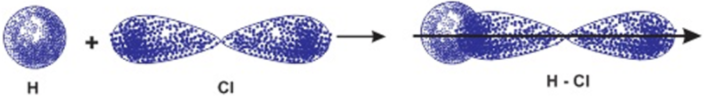
Giải thích sự hình thành liên kết cộng hóa trị bằng sự xen phủ các obitan trong phân tử HCl.
Giải
Liên kết hóa học trong phân tử hợp chất HCl được hình thành nhờ sự xen phủ giữa obitan 1s của nguyên tử hiđro và obitan 3p có 1 electron độc thân của nguyên tử clo.
Bài 5 trang 75 SGK Hóa học 10 Nâng cao
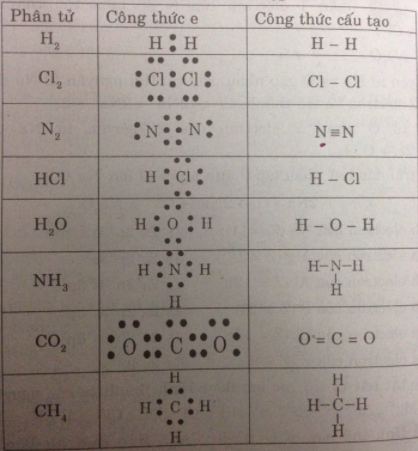
Hãy viết công thức electron và công thức cấu tạo của các phân tử sau đây:
\({H_2},HCl,{H_2}O,C{l_2},N{H_3},C{H_4}.\)
Giải
Bài 6 trang 75 SGK Hóa học 10 Nâng cao
X, Y, Z là những nguyên tố có số đơn vị điện tích hạt nhân là 9, 19, 8.
a) Viết cấu hình electron nguyên tử các nguyên tố đó.
b) Dự đoán kiểu liên kết hóa học có thể có giữa các cặp X và Y, Y và Z, Z và X.
Giải
a) Cấu hình electron nguyên tử là:
\(\eqalign{& X\,\left( {Z = 9} \right):\,\,1{s^2}2{s^2}2{p^5} \cr& Y\left( {Z = 19} \right):\,\,1{s^2}2{s^2}2{p^6}3{s^2}3{p^6}4{s^1} \cr& Z\left( {Z = 8} \right):\,\,1{s^2}2{s^2}2{p^4} \cr} \)
b) Liên kết giữa X và Y, Y và Z là liên kết ion.
Liên kết giữa X và Z là liên kết cộng hóa trị có cực.
Giaibaitap.me
Giải bài tập trang 80 bài 18 Sự lai hóa các obitan nguyên tử. Sự hình thành liên kết đơn, liên kết đôi và liên kết ba Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Thế nào là sự lai hóa...
Giải bài tập trang 82 bài 19 Luyện tập về: Liên kết ion. Liên kết cộng hóa trị. Sự lai hóa các obitan nguyên tử Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Trình bày nội dung các quy tắc bát tử. ...
Giải bài tập trang 85 bài 20 Tinh thể nguyên tử. Tinh thể phân tử Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Tìm câu sai...
Giải bài tập trang 87 bài 21 Hiệu độ âm điện và liên kết hóa học Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Chọn câu đúng trong các câu sau...
