Bài 1 trang 82 SGK Hóa học 10 Nâng cao
Trình bày nội dung các quy tắc bát tử. Vận dụng quy tắc bát tử để giải thích sự hình thành liên kết ion trong các phân tử: Li, KBr, , \(CaC{l_2}.\)
Giải
Quy tắc bát tử: Nguyên tử của nguyên tố có khuynh hướng liên kết với các nguyên tử khác để đạt được cấu hình electron bền vững của các khí hiếm với 8 electron (hoặc 2 electron đối với heli) ở lớp ngoài cùng.
Sự hình thành liên kết trong LiF, KBr, \(CaC{l_2}\) được giải thích ngắn gọn bằng sơ đồ sau:
\(\eqalign{ &LiF:\,\,\,\,\,\,Li\,\,\,\,\, + \,\,\,\,\,\,F\,\,\,\,\,\,\,\, \to \,\,\,\,\,L{i^ + }+ \,\,\,{F^ - }\,\,\,\to LiF. \cr & \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,1{s^2}2{s^1}\,\,\,\,\,\,1{s^2}2{s^2}2{p^5}\,\,\,\,\,\,\,\,\,\,\,1{s^2}\,\,\,\,\,\,1{s^2}2{s^2}2{p^6} \cr& KBr:\,K\,\,\,+ \,\,\,\,\,Br\,\,\,\,\,\,\,\,\,\,\,\, \to \,\,\,\,{K^ + }\,\,\,\,+ \,\,B{r^ - } \to KBr \cr& \,\,\,\,\,\,\,\,\,\,\,\left[ {Ar} \right]4{s^1}\,\,\,\left[ {Ar} \right]3{d^{10}}4{s^2}4{p^5}\,\,\,\,\left[ {Ar} \right]\,\,\,\,\,\,\,\left[ {Kr} \right] \cr} \)
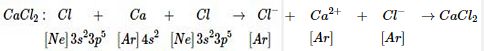
Bài 2 trang 82 SGK Hóa học 10 Nâng cao
Sử dụng mô hình xen phủ các obitan nguyên tử để giải thích sự hình thành liên kết cộng hóa trị các phân tử: \({I_2},HBr.\)
Giải
- Liên kết hóa học trong \(I_2\) được hình thành nhờ sự xen phủ giữa obitan p chứa electron độc thân của mỗi nguyên tử iot.
Sơ đồ:

- Liên kết hóa học trong phân tử HBr được hình thành nhờ sự xen obitan 1s của nguyên tử hiđro và obitan 4p có 1 electron độc nguyên tử brom.
Sơ đồ:

Bài 3 trang 82 SGK Hóa học 10 Nâng cao
Hãy viết công thức electron và công thức cấu tạo của các phân tử sau: \(P{H_3},S{O_2}HN{O_3},{C_4}{H_{10}}.\)
Giải
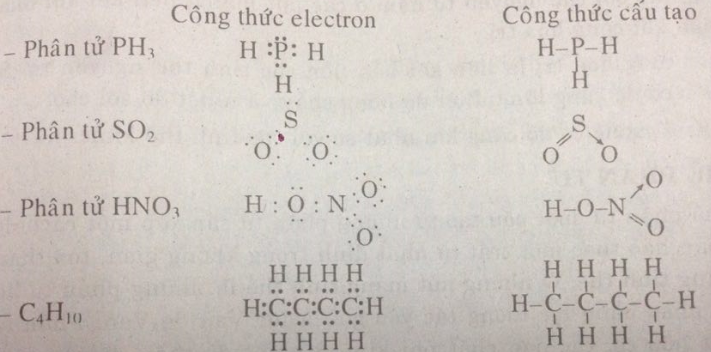
Hay
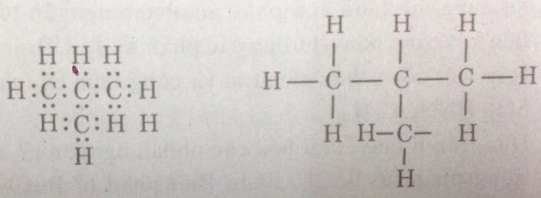
Bài 4 trang 82 SGK Hóa học 10 Nâng cao
Dựa trên lí thuyết lai hóa các obitan nguyên tử, mô tả sự hình thành liên kết trong các phân tử: \(BeC{l_2},BC{l_3}.\) Biết phân tử \(BeC{l_2}\) có dạng đường thẳng, còn phân tử \(BC{l_3}\) có dạng tam giác đều.
Giải
- Phân tử \(BeC{l_2}\); Nguyên tử Beri đã sử dụng 1 AOs và 2 Aop lai hóa với nhau để tạo thành hai obitan lai hóa sp nằm thẳng hàng với nhau về 2 phía đối xứng nhau. Beri đã sử dụng 2 obitan lai hóa sp xen phủ với 2 obitan p của 2 nguyê tử clo, tạo thành liên kết \(\sigma \) giữa Be – Cl.
- Phân tử \(BC{l_3}\): Nguyên tử bo đã sử dụng 1 Aos và 2 AOp lại hóa với nhau để tạo thành 3 AO lai hóa sp2 nằm trong ột mặt phẳng định hướng từ tâm đến 3 đỉnh của tam giác đều. Nguyên tử bo đã sử dụng 3 obitan lai hóa sp2 xen phủ với 3 obitan p của 3 nguyên tử clo tạo thành 3 liên kết \(\sigma \) giữa B – Cl.
Giaibaitap.me
Giải bài tập trang 85 bài 20 Tinh thể nguyên tử. Tinh thể phân tử Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Tìm câu sai...
Giải bài tập trang 87 bài 21 Hiệu độ âm điện và liên kết hóa học Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Chọn câu đúng trong các câu sau...
Giải bài tập trang 90 bài 22 Hóa trị và số oxi hóa Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Số oxi hóa của nitơ trong...
Giải bài tập trang 92 bài 23 Liên kết kim loại Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Hãy cho một thí dụ về mạng tinh thể kim loại ...
