Bài 1 trang 102 SGK Hóa học 10 Nâng cao
Một nguyên tử lưu huỳnh (S) chuyển thành ion sunfua \(\left( {{S^{2 - }}} \right)\) bằng cách:
A. nhận thêm một electron.
B. nhường đi một electron.
C. nhận thêm một electron.
D. nhường đi hai electron.
Hãy tìm đáp án đúng.
Giải
Chọn C.
loigiaihay.com
Bài 2 trang 103 SGK Hóa học 10 Nâng cao
Trong phản ứng: \(C{l_2} + 2KBr \to B{r_2} + 2KCl,\) nguyên tố clo
A. chỉ bị oxi hóa.
B. bị khử.
C. không bị oxi hóa, cũng không bị khử.
D. vừa bị oxi hóa, vừa bị khử.
Hãy tìm đáp án đúng.
Giải
\(Cl_2^0 + 2e\,\, \to \,\,2\mathop {Cl}\limits^ - \) : sự khử \( \Rightarrow C{l_2}\) là chất oxi hóa (chất bị khử).
Chọn B.
loigiaihay.com
Bài 3 trang 103 SGK Hóa học 10 Nâng cao
Trong phản ứng: \(2Fe{\left( {OH} \right)_3} \to F{e_2}{O_3} + 3{H_2}O\), nguyên tố sắt
A. bị oxi hóa
B. bị khử.
C. không bị oxi hóa, cũng không bị khử.
D. vừa bị oxi hóa, vừa bị khử.
Hãy tìm đáp án đúng.
Giải
Vì số oxi hóa của Fe trước và sau phản ứng không đổi nên không bị oxi hóa, cũng không bị khử.
Chọn C.
loigiaihay.com
Bài 4 trang 103 SGK Hóa học 10 Nâng cao
Các câu sau đây đúng hay sai?
a) Sự đốt cháy natri trong khí clo là một phản ứng oxi hóa – khử.
b) \(N{a_2}O\) bao gồm các ion \(N{a^{2 + }}\) và \({O^{2 - }}\).
c) Khi tác dụng với CuO, CO là chất khử.
d) Sự oxi hóa ứng với sự giảm số oxi hóa của một nguyên tố
e) Sự khử ứng với sự tăng số oxi hóa của một nguyên tố.
Giải
Câu đúng là a, c. Câu sai là b, d, e.
loigiaihay.com
Bài 5 trang 103 SGK Hóa học 10 Nâng cao
Tính số oxi hóa của:
a) cacbon trong \(C{H_4},CO,C,C{O_2},CO_3^{2 - },HCO_3^ - \)
b) lưu huỳnh trong \(S{O_2},{H_2}S{O_3},{S^{2 - }},S,SO_3^{2 - },HSO_4^ - ,H{S^ - }.\)
c) clo trong \(ClO_4^ - ,Cl{O^ - },C{l_2},C{l^ - },ClO_3^ - ,C{l_2}{O_7}\)
Giải
a) Số oxi hóa của cacbon: \(\mathop C\limits^{ + 4} {H_4},\,\,\mathop C\limits^{ + 2} O,\,\,\mathop C\limits^0 ,\,\,\mathop C\limits^{ + 4} {O_2},\,\,\mathop C\limits^{ + 4} O_3^{2 - },\,\,H\mathop C\limits^{ + 4} O_3^ - \)
b) Số oxi hóa của lưu huỳnh: \(\mathop S\limits^{ + 4} {O_2},\,\,{H_2}\mathop S\limits^{ + 4} {O_3},\,\,\mathop {{S^{2 - }}}\limits^{ - 2} ,\,\,\mathop S\limits^0 ,\,\,\mathop S\limits^{ + 4}{O_3}^{2-} ,\,\,H\mathop S\limits^{ + 6} O_4^ - ,H\mathop {{S^ - }}\limits^{ - 2} .\)
c) Số oxi hóa của clo: \(\mathop {Cl}\limits^{ + 7} O_4^ - ,\,\,\mathop {Cl}\limits^{ + 1} {O^ - },\,\,\mathop {C{l_2}}\limits^0 ,\,\,\mathop {C{l^ - }}\limits^{ - 1} ,\,\,\mathop {Cl}\limits^{ + 5} O_3^ - ,\,\,\mathop {C{l_2}}\limits^{ + 7} {O_7}.\)
loigiaihay.com
Bài 6 trang 103 SGK Hóa học 10 Nâng cao
Lập các phương trình hóa học của phản ứng oxi hóa – khử theo các sơ đồ dưới đây và xác định vai trò của từng chất trong phản ứng:
\(\eqalign{ & a)\,\,N{a_2}S{O_3} + KMn{O_4} + {H_2}O \to N{a_2}S{O_4}\cr& \;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;+ Mn{O_2} + KOH \cr & b)\,\,FeS{O_4} + {K_2}C{r_2}{O_7} + {H_2}S{O_4} \to F{e_2}{\left( {S{O_4}} \right)_3} \cr&\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;+ {K_2}S{O_4} + C{r_2}{\left( {S{O_4}} \right)_3} + {H_2}O \cr & c)\,\,Cu + HN{O_3} \to Cu{\left( {N{O_3}} \right)_2} + N{O_2} + {H_2}O \cr & d)\,\,Cu + HN{O_3} \to Cu{\left( {N{O_3}} \right)_2} + NO + {H_2}O \cr & e)\,\,F{e_3}{O_4} + HN{O_3} \to Fe{\left( {N{O_3}} \right)_3} + NO + {H_2}O \cr & g)\,\,Fe + {H_2}S{O_4} \to F{e_2}{\left( {S{O_4}} \right)_3} + S{O_2} + {H_2}O \cr & h)\,\,C{l_2} + NaOH \to NaCl + NaClO + {H_2}O \cr} \)
Giải


loigiaihay.com
Bài 7 trang 104 SGK Hóa học 10 Nâng cao
Điiot pentaoxit \(\left( {{I_2}{O_5}} \right)\) tác dụng với cacbon monooxit tạo ra cacbon ddiooxit và iot.
a) Lập phương trình hóa học của phản ứng oxi hóa – khử trên.
b) Khi cho 1 lít hỗn hợp khí có chứa CO và \(C{O_2}\) tham gia phản ứng thì khối lượng điiot pentaoxit bị khử là 0,50g. Tính thành phần phần trăm về thể tích của CO trong hỗn hợp khí. Biết rằng ở điều kiện thí nghiệm, thể tích mol của chất khí V = 24 lít.
Giải
a) Phương trình phản ứng: \({I_2}\mathop {{O_5}}\limits^{ + 5} + \mathop C\limits^{ + 2} O\,\, \to \,\,\mathop C\limits^{ + 4} {O_2} + \mathop {{I_2}}\limits^0 \)
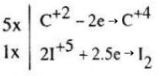
\( {I_2}{O_5} + 5CO\,\, \to \,\,5C{O_2} + {I_2}. \)
b) Tính phần trăm về thể tích CO trong hỗn hợp khí:
Gọi x là số mol của CO, y là số mol của CO2 có trong 1 lít hỗn hợp.
Ta có \(x + y = {1 \over {24}}\,\,\,\left( 1 \right)\)
Chỉ có CO tham gia phản ứng. Theo phương trình phản ứng:
\({n_{CO}} = 5{n_{{I_2}{O_5}}} = {{5.0,5} \over {334}} = x\)
Ta có: \(\% {V_{CO}} = \% {n_{CO}} = {{2,5} \over {334}}.24.100 \approx 18\% .\)
loigiaihay.com
Giải bài tập trang 109, 110 bài 26 Phân loại phản ứng trong hóa học vô cơ Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Trong các phản ứng hóa hợp dưới đây, phản ứng nào là phản ứng oxi hóa – khử...
Giải bài tập trang 112 bài 27 luyện tập chương IV - phản ứng hóa học Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: Trong phản ứng hóa học sau...
Giải bài tập trang 113 bài 27 luyện tập chương IV - phản ứng hóa học Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 6: Hãy nêu thí dụ về phản ứng tạo ra muối...
Giải bài tập trang 119 bài 29 Khái quát về nhóm Halogen Sách giáo khoa (SGK) Hóa học 10 Nâng cao. Câu 1: So sánh cấu tạo electron của nguyên tử các nguyên tố flo, clo, brom, iot...
