Bài 1 - Trang 148 - SGK Hóa học 9
Cho các chất sau : rượu etylic, axit axetic, chất béo. Hỏi :
a) Phân tử chất nào có nhóm – OH ? Nhóm –COOH ?
b) Chất nào tác dụng được với K ; Zn ; NaOH ; K2CO3 ?
Viết các phương trình phản ứng hóa học.
Lời giải.
a) Chất có nhóm –OH là rượu etylic, chất có nhóm –COOH là axit axetic.
b) Chất tác dụng được với K là rượu etylic và axit axetic :
2C2H5OH + 2Na -> C2H5ONa + H2
2CH3 – CH2OH + 2Na -> 2CH3 – CH2ONa + H2
Chất tác dụng được với Zn, K2CO3 là axit axetic :
2CH3 – CH2OH + Zn -> 2CH3 – CH2ONa + H2O
2CH3 – CH2OH + K2CO3 -> 2CH3 – CH2OK + CO2 + H2O
Chất tác dụng được với NaOH là axit axetic và chất béo :
CH3 – CH2OH + NaOH -> CH3 – CH2ONa + H2O
(RCOO)3C3H5 + NaOH -> 3RCOONa + C3H5(OH)3
Bài 2 - Trang 148 - SGK Hóa học 9
Tương tự chất béo, etyl axetat cũng có phản ứng thủy phân trong dung dịch axit và dung dịch kiềm. Hãy viết phương trình hóa học của phản ứng xảy ra khi đun etyl axetat với dung dịch HCl, dung dịch NaOH.
Bài làm.
Các phương trình hóa học :
CH3COOC2H5 + H2O ![]() CH3COOH + C2H5OH.
CH3COOH + C2H5OH.
CH3COOC2H5 + NaOH \(\overset{t^{o}}{\rightarrow}\) CH3COONa + C2H5OH.
Bài 3 trang 149 sgk hóa học 9
Hãy chọn các chất thích hợp điền vào dấu hỏi rồi viết các phương trình hóa học của các sơ đồ phản ứng sau:
a) C2H5OH + ?--------> ? + H2
b) C2H5OH + ? ------ > CO2 + ?

Giải
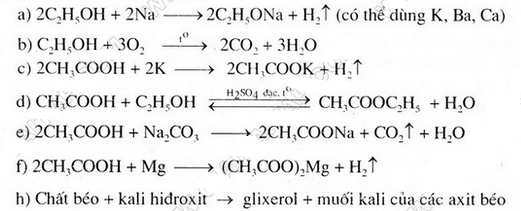
Bài 4 - Trang 149 - SGK Hóa học 9
Có ba lọ không nhãn đựng ba chất lỏng là : rượu etylic, axit axetic, dầu ăn tan trong rượu etylic. Chỉ dùng nước và quỳ tím, hãy phân biệt các chất lỏng trên.
-Dùng quỳ tím để nhận biết ra axit axetic.
-Hai chất lỏng còn lại cho vào ống nghiệm đựng nước, chất nào tan hoàn toàn tạo thành hỗn hợp đồng chất là rượu etylic, chất nào không tan nổi lên trên, hỗn hợp tách thành hai lớp riêng biệt là dầu ăn.
Bài 5 - Trang 149 - SGK Hóa học 9
Khi xác định công thức các chất hữu cơ A và B, người ta thấy công thức phân tử của A là C2H6O, còn công thức phân tử của B là C2H4O2. Để chứng minh A là rượu etylic, B là axit axetic cần phải làm thêm những thí nghiệm nào ? Viết phương trình hóa học để minh họa.
Hướng dẫn.
+ Ứng với công thức phân tử C2H6O2 có 2 chất có công thức cấu tạo khác nhau là:
CH3 - CH2 - OH (1) và CH3 – O – CH3 (2).
Vì vậy, để chứng minh ( hay xác định) A là rượu etylic thì ta phải xác định công thức cấu tạo của nó :
Cho A tác dụng với Na, nếu có H2 thoát ra, suy ra phân tử có nhóm –OH, là rượu etylic.
2CH3 – CH2 – OH + 2Na -> 2CH3 – CH2 – ONa + H2
Chất đi metyl ete CH3 – O – CH3 không phản ứng với Na.
+ Ứng với công thức phân tử C2H4O2 có đến ba chất khác nhau.
CH3 – COOH (1) ; HCOO – CH (2) và ![]()
Vì vậy để xác định B là axit axetic ta phải xác định công thức cấu tạo của nó :
Cho A tác dụng với muối cacbonat, thí dụ Na2CO3, nếu có khí CO2 thoát ra, suy ra phân tử có nhóm –COOH, là axit axetic.
2CH3 – COOH + Na2CO3 -> 2CH3 – COONa + CO2 + H2O.
Bài 6 - Trang 149 - SGK Hóa học 9
Khi lên men dung dịch loãng của rượu etylic, người ta được giấm ăn.
a) Từ 10 lít rượu 8o có thể tạo ra được bao nhiêu gam axit axetic ? Biết hiệu suất quá trình lên men là 92% và rượu etylic có D = 0,8g/cm3.
b)Nếu pha khối lượng axit axetic trên thành dung dịch giấm 4% thì khối lượng dung dịch giấm thu được là bao nhiêu.
Hướng dẫn.
a)\(V_{C_{2}H_{5}OH}=V_{dd}.\frac{8}{100}=10.\frac{8}{100}=0,8\) = 800 ml.
\(m_{C_{2}H_{5}OH}=\) V. D = 800.0,8 = 640 gam.
Phản ứng lên men rượu :
C2H5OH + O2 -> CH3COOH + H2O
46 60 (gam)
640 m? (gam)
Khối lượng axit thu được theo lí thuyết \(m=\frac{640.60}{46}\) (gam).
Vì hiệu suất của phản ứng chỉ đạt 92% nên khối lượng CH3COOH thực thế thu được là:
\(m_{CH_{3}COOH}=\frac{640.60}{46}.\frac{92}{100}\) = 768 (gam).
b) Khối lượng dung dịch giấm ăn CH3COOH 4% thu được là :
\(m_{dd}=768.\frac{100}{4}=19200\)
Bài 7 - Trang 149 - SGK Hóa học 9
Cho 100 gam dung dịch CH3COOH 12% tác dụng vừa đủ với dung dịch NaHCO3 8,4%.
a) Hãy tính khối lượng NaHCO3 đã dùng.
b) Hãy tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng.
Hướng dẫn.
a) Số mol CH3COOH = 0,2 mol.
CH3 – COOH + NaHCO3 -> CH3 – COONa + CO2 + H2O
0,2 0,2 0,2 0,2
Khối lượng NaHCO3 cần dùng là ; 0,2.84 = 16,8 gam.
\(m_{dd_{NaHCO_{3}}}=16,8\frac{100}{8,4}=200\) (gam).
b)
\(m_{c.t}=m_{CH_{3}COONa}\) = 0,2.82 = 16,4 (gam).
=> \(m_{dd}=m_{dd_{CH_{3}COOH}}+m_{dd_{NaHCO_{3}}}-m_{CO_{2}}\)
= 100 + 200 - (0,2.44) = 291,2 (gam).
=> C% (CH3 – COONa) = \(\frac{16,4}{291,2}\).100% = 5,63%.
Giaibaitap.me
Giải bài tập trang 152 bài 50 Glucozơ Sách giáo khoa (SGK) Hóa học 9. Câu 1: Hãy kể tên một số loại quả chín có chứa glucozơ...
Giải bài tập trang 155 bài 51 Saccarozơ Sách giáo khoa (SGK) Hóa học 9. Câu 1: Khi pha nước giải khát có nước đá người ta có thể làm như sau...
Giải bài tập trang 158 bài 52 Tinh bột và xenlulozơ Sách giáo khoa (SGK) Hóa học 9. Câu 1: Chọn từ thích hợp (xenlulozơ hoặc tinh bột) rồi điền vào các chỗ trống...
Giải bài tập trang 160 bài 53 Protein Sách giáo khoa (SGK) Hóa học 9. Câu 1: Hãy điền những từ hoặc cụm từ thích hợp vào các dấu chấm...
