Bài tập trắc nghiệm 2.46, 2.47 trang 19 sách bài tập(SBT) hóa học 11
2.46. Khí nitơ có thể được tạo thành trong các phản ứng hoá học nào sau đây ?
A. Đốt cháy NH3 trong oxi có mặt chất xúc tác platin
B. Nhiệt phân NH4NO3
C. Nhiệt phân AgNO3
D. Nhiệt phân NH4NO2
2.47. Cặp chất nào sau đây có thể tồn tại trong cùng một dung dịch ?
A. Axit nitric và đồng(II) nitrat
B. Đồng(II) nitrat và amoniac
C. Bari hiđroxit và axit photphoric.
D. Amoni hiđrophotphat và kali hiđroxit
Hướng dẫn trả lời:
2.46. D
2.47. A
Bài tập trắc nghiệm 2.48 trang 20 sách bài tập(SBT) hóa học 11
2.48. Hoà tan 12,8 g kim loại hoá trị II trong một lượng vừa đủ dung dịch \(HN{O_3}\) 60% (D = 1,365 g/ml), thu được 8,96 lít (đktc) một khí duy nhất màu nâu đỏ. Tên của kim loại và thể tích dung dịch \(HN{O_3}\) đã phản ứng là
A. đồng ; 61,5 ml.
B. chì ; 65,1 ml.
C. thuỷ ngân ; 125,6 ml.
D. sắt; 82,3 ml.
Hướng dẫn trả lời:
2.48. A
\(M + 4HN{O_3} \to M{(N{O_3})_2} + 2N{O_2} \uparrow + 2{H_2}O\)
(màu nâu đỏ)
Số mol khí \(N{O_2}\) : \(\frac{{8,96}}{{22,4}}\) = 0,4 (mol).
Theo phương trình hoá học :
\({n_M}\) = 0,2 mol và \({n_{HN{O_3}}} = \frac{{0,4.4}}{2}\) = 0,8 (mol).
Khối lượng mol nguyên tử của kim loại M :
M = \(\frac{{12,8}}{{0,2}} = 64(g/mol)\)
\( \Rightarrow \) kim loại là Cu (đồng).
Gọi V (ml) là thể tích của dung dịch HNO3 60%. Ta có phương trình liên hệ V với \({n_{HN{O_3}}}\) :
\(\frac{{V.1,365.60}}{{100.63}} = 0,8 \Rightarrow V = 61,5ml\)
Bài tập 2.49 trang 20 sách bài tập(SBT) hóa học 11
2.49. Viết các phương trình hoá học thực hiện các dãy chuyển hoá sau :
1. \(N{H_4}Cl\)![]()
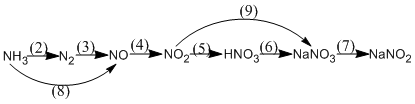
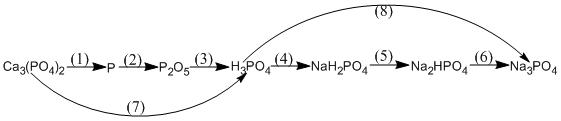
2. 
Hướng dẫn trả lời:
1. (1) \(N{H_4}Cl + NaOH \to N{H_3} + {H_2}O + NaCl\)
(2) \(4N{H_3} + 3{O_2}\)![]() \(2{N_2} + 6{H_2}O\)
\(2{N_2} + 6{H_2}O\)
(3) \({N_2} + {O_2}\)![]() 2NO
2NO
(4) \(2NO + {O_2} \to 2N{O_2}\)
(5) \(4N{O_2} + {O_2} + 2{H_2}O \to 4HN{O_3}\)
(6) \(HN{O_3} + NaOH \to NaN{O_3} + {H_2}O\)
(7) \(2NaN{O_3}\)![]() \(2NaN{O_2} + {O_2}\)
\(2NaN{O_2} + {O_2}\)
(8) \(4N{H_3} + 5{O_2}\)![]() \(4NO + 6{H_2}O\)
\(4NO + 6{H_2}O\)
(9) \(2N{O_2} + 2NaOH \to NaN{O_3} + NaN{O_2} + {H_2}O\)
2. (1) \(C{a_3}{(P{O_4})_2} + 3Si{O_2} + 5C\)![]() \(2P + 3CaSi{O_3} + 5CO\)
\(2P + 3CaSi{O_3} + 5CO\)
(2) \(4P + 5{O_2}\)![]() \(2{P_2}{O_5}\)
\(2{P_2}{O_5}\)
(3) \({P_2}{O_5} + 3{H_2}O \to 2{H_3}P{O_4}\)
(4) \({H_3}P{O_4} + NaOH \to Na{H_2}P{O_4} + {H_2}O\)
(5) \(Na{H_2}P{O_4} + NaOH \to N{a_2}HP{O_4} + {H_2}O\)
(6) \(N{a_2}HP{O_4} + NaOH \to N{a_3}P{O_4} + {H_2}O\)
(7) \(C{a_3}{(P{O_4})_2} + 3{H_2}S{O_4} \to 2{H_3}P{O_4} + 3CaS{O_4}\)
(8) \({H_3}P{O_4} + 3NaOH \to N{a_3}P{O_4} + 3{H_2}O\)
Giaibaitap.me
Giải bài tập trang 20 bài 13 luyện tập tính chất của nito, photpho và các hợp chất của chúng Sách bài tập hóa học 11. Câu 2.50: Viết phương trình hoá học ở dạng phân tử và dạng ion rút gọn của phản ứng xảy ra trong dung dịch giữa các chất sau...
Giải bài tập trang 21, 22 bài 15 cacbon Sách bài tập (SBT) hóa học 11. Câu 3.1: Trong những nhận xét dưới đây, nhận xét nào không đúng ?...
Giải bài tập trang 22, 23 bài 16 hợp chất của cacbon Sách bài tập (SBT) hóa học 11. Câu 3.6: Cần thêm ít nhất bao nhiêu ml dung dịch Na2CO3 0,15M vào 25 ml dung dịch Al2(SO4)3 0,02M để...
Giải bài tập trang 23, 24 bài 17 silic và hợp chất của silic Sách bài tập (SBT) hóa học 11. Câu 3.11: Natri silicat có thể được tạo thành bằng cách...
