Bài tập 9.18 trang 66 sách bài tập(SBT) hóa học 11
9.18. Viết công thức cấu tạo và tên tất cả các axit cacboxylic có cùng công thức phân tử C5H10O2.
Hướng dẫn trả lời:
CH3 - CH2 - CH2 - CH2 - COOH ( axit pentanoic )
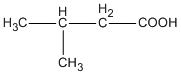 ( axit 3-metylbutanoic )
( axit 3-metylbutanoic )
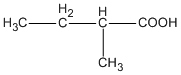 ( axit 2-metylbutanoic )
( axit 2-metylbutanoic )
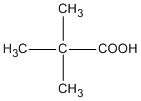 ( axit 2,2-đimetylpropanoic )
( axit 2,2-đimetylpropanoic )
Bài tập 9.19 trang 67 sách bài tập(SBT) hóa học 11
9.19. Người ta có thể điều chế axit axetic xuất phát từ một trong các hiđrocacbon dưới đây (cùng với các chất vô cơ cần thiết) :
1. metan ;
2. etilen ;
3. axetilen ;
4. butan.
Hãy viết phương trình hoá học của phản ứng xảy ra trong các quá trình đó, có ghi rõ điểu kiện phản ứng.
Hướng dẫn trả lời:
1. Từ \(C{H_4}\)
\(2C{H_4}\) ![]()
![]() + \(3{H_2}\)
+ \(3{H_2}\)
![]() + \({H_2}O\)
+ \({H_2}O\) ![]()
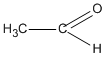
\(2C{H_3} - CHO + {O_2}\) ![]() \(2C{H_3}COOH\)
\(2C{H_3}COOH\)
2. Từ \({C_2}{H_4}\)
\({C_2}{H_4} + HOH\) ![]() \(C{H_3} - C{H_2} - OH\)
\(C{H_3} - C{H_2} - OH\)
\({C_2}{H_5}OH + {O_2}\) ![]() \(C{H_3}COOH + {H_2}O\)
\(C{H_3}COOH + {H_2}O\)
3. Từ \({C_2}{H_2}\) : Hai phản ứng cuối ở phần 1.
4. Từ \({C_4}{H_{10}}\) :
\(2C{H_3} - C{H_2} - C{H_2} - C{H_3} + 5{O_2}\) ![]() \(4C{H_3}COOH + 2{H_2}O\)
\(4C{H_3}COOH + 2{H_2}O\)
Bài tập 9.20 trang 67 sách bài tập(SBT) hóa học 11
9.20. Dung dịch axit fomic 0,092% có khối lượng riêng xấp xỉ 1 g/ml. Trong dịch đó, chỉ có 5,0% số phân tử axit fomic phân li thành ion.
Hãy tính pH của dung dịch đó.
Hướng dẫn trả lời:
9.20. Khối lượng của 1 lít (1000 ml) dung dịch axit fomic 0,092% là 1000 g. trong đó khối lượng của axit fomic là :
\(1000.\frac{{0,092}}{{100}} = 0,92(g)\)
và số mol axit fomic là : \(\frac{{0,92}}{{46}}\) = 0,02 (mol).
Số mol axit fomic phân li thành ion là : \(0,02.\frac{5}{{100}}\) = 0,001 (mol).
\(HCOOH \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over
{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} HCO{O^ - } + {H^ + }\)
0,001 mol 0,001 mol
Nồng độ [H+] = 0,001 mol/l = \({1.10^{ - 3}}\) mol/l. Vậy pH = 3.
Giaibaitap.me
Giải bài tập trang 68 bài 45 axit cacboxylic Sách bài tập (SBT) hóa học 11. Câu 9.24: Chất A là một axit cacboxylic đơn chức, dẫn ,xuất của anken...
Giải bài tập trang 68 bài 46 luyện tập andehit - xeton - axit cacboxylic Sách bài tập (SBT) hóa học 11. Câu 9.27: Trong các nhận xét dưới đây, nhận xét nào không đúng ?...
Giải bài tập trang 69, 70 bài 46 luyện tập andehit - xeton - axit cacboxylic Sách bài tập (SBT) hóa học 11. Câu 9.31: Viết phương trình hóa học thực hiện các biến đổi dưới đây. Các chất hữu cơ được viết dưới dạng công thức cấu tạo và ghi tên...
Giải bài tập trang 70, 71 bài 46 luyện tập andehit - xeton - axit cacboxylic Sách bài tập (SBT) hóa học 11. Câu 9.36: Viết phương trình hoá học thưc hiện các biến hoá dưới đây (mỗi mũi tên là một phản ứng)...
