Câu 1 trang 47 SGK Hóa học 11 Nâng cao
Mô tả và giải thích hiện tượng xảy ra trong thí nghiệm chứng minh amoniac tan nhiều trong nước.
Giải
Nạp đầy khí \(NH_3\) vào bình thủy tinh trong suốt, đậy bình bằng ống cao su có ống thủy tinh vuốt nhọn xuyên qua. Nhúng dần ống thủy tinh vào một chậu thủy tinh chứa nước có pha vài giọt dung dịch phenolphtalein, ta thấy nước trong chậu phun vào bình thành những tia màu hồng. Đó là do khí \(NH_3\) tan nhiều trong nước làm giảm áp suất trong bình và nước bị hút vào bình. Tia nước có màu hồng chứng tỏ dung dịch có tính bazơ
Câu 2 trang 47 SGK Hóa học 11 Nâng cao
Có 5 bình đựng khí riêng biệt 5 chất khí: \({N_2},{O_2},N{H_3},C{l_2}\) và \(C{O_{{2 }}}\). Hãy đưa ra một thí nghiệm đơn giản để nhận ra bình đựng khí \(N{H_3}\).
Giải
Cách 1: Dùng đũa thủy tinh nhúng vào lọ đựng dung dịch HCl và đưa bào lần lượt các bình mất nhãn trên nếu có khói trắng xuất hiện là bình chứa khí \(N{H_3}:N{H_3} + HCl \to N{H_4}Cl\) (rắn) khói trắng.
Cách 2: Dùng giấy quỳ tẩm nước cho tiếp xúc với miệng các bình khí. Ở bình nào làm quỳ tím hóa xanh là \(N{H_3}\)
Câu 3 trang 47 SGK Hóa học 11 Nâng cao
Nêu tính chất hóa học đặc trưng và những ứng dụng của amoniac. Tại sao người ta nó amoniac là một bazơ yếu ?
Giải
a) Tính chất hóa học của \(N{H_3}\)
Tính bazơ yếu:
![]()
\(N{H_3} + HCl \to NH_4Cl\) (bốc khói trắng)
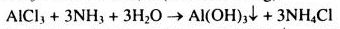
\(Cu{(N{O_3})_2} + 2N{H_3} + {H_2}O \to Cu{\left( {OH} \right)_2} \downarrow \)
\(+ 2N{H_4}N{O_3}\)
\(Cu{(OH)_2} + 4N{H_3} \to {\rm{[}}Cu{\left( {N{H_3}} \right)_4}{\rm{]}}{\left( {OH} \right)_2}\) Dung dịch xanh thẫm
Tính khử:
![]()
\((2\mathop N\limits^{ - 3} - 6e \to {N_2})\)
\(2N{H_3} + 3C{l_2} \to {N_2} + 6HCl \)
\((2\mathop N\limits^{ - 3} - 6e \to {N_2})\)
\(4N{H_3} + 5{O_2} \to 4NO + 6{H_2}O \)
\((\mathop N\limits^{ - 3} - 5e \to \mathop N\limits^{ + 2} )\)
\(4N{H_3} + 3{O_2} \to 2{N_2} + 6{H_2}O \)
\((2\mathop N\limits^{3 - } - 6e \to {N_2})\)
b) Ứng dụng
- \(N{H_3}\) được sử dụng để sản xuất \(HN{O_3}\), phân bón, điều chế \({N_2}{H_4}\) làm nhiên liệu cho tên lửa.
- \(N{H_3}\) lỏng được dùng làm chất gây lạnh trong máy lạnh.
c) \(N{H_3}\) là một bazơ yếu.
Với cùng nồng độ thì \(O{H^ - }\) do \(N{H_3}\) tạo thành nhỏ hơn nhiều so với NaOH, \(N{H_3}\) bị bazơ đẩy ra khỏi dung dịch muối \(\Rightarrow \) \(N{H_3}\) là một bazơ yếu.
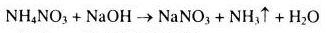
Câu 4 trang 47 SGK Hóa học 11 Nâng cao
Dung dịch amoniac có thể hòa tan được \(Zn{(OH)_2}\) là do
A. \(Zn{(OH)_2}\) là hiđoxit lưỡng tính.
B. \(Zn{(OH)_2}\) là một bazơ ít tan.
C. \(Zn{(OH)_2}\) có khả năng tạo thành phức chất tan, tương tự như \(Cu{(OH)_2}\).
D. \(N{H_3}\) là một hợp chất có cực và là một bazơ yếu.
Giải
\(Zn{(OH)_2} + 4N{H_3} \to \left[ {Zn{{(N{H_3})}_4}} \right]{\left( {OH} \right)_2}\)
Chọn đáp án C
Giaibaitap.me
Giải bài tập trang 47 bài 11 Amoniac và amoni SGK Hóa học 11 Nâng cao. Câu 5: Viết phương trình hóa học của các phản ứng thực hiện sơ đồ chuyển hóa sau...
Giải bài tập trang 55 bài 12 axit nitric và muối nitrat SGK Hóa học 11 Nâng cao. Câu 1: Viết công thức electron và công thức cấu tạo axit nitic và cho biết nguyên tố nitơ có số oxi hóa là bao nhiêu...
Giải bài tập trang 55 bài 12 axit nitric và muối nitrat SGK Hóa học 11 Nâng cao. Câu 5: Tại sao khi điều chế axit nitric bốc khói phải sử dụng...
Giải bài tập trang 57 bài 13 luyện tập tính chất của nito và hợp chất của nito SGK Hóa học 11 Nâng cao. Câu 1: Viết các phương trình hóa học để thực hiện các sơ đồ chuyển hóa sau...
