Câu 5 trang 47 SGK Hóa học 11 Nâng cao
Viết phương trình hóa học của các phản ứng thực hiện sơ đồ chuyển hóa sau:
![]()
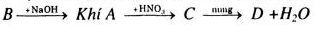
Giải
Khí A là \(N{H_3}\)
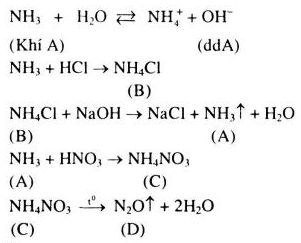
Câu 6 trang 47 SGK Hóa học 11 Nâng cao
Cho cân bằng hóa học sau:
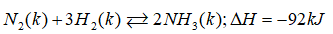
Cân bằng trên sẽ dịch chuyển theo chiều nào (có giải thích) khi:
a) tăng nhiệt độ
b) hóa lỏng amoniac để tách amoniac ra khỏi hỗn hợp phản ứng
c) giảm thể tích của hệ phản ứng
Giải
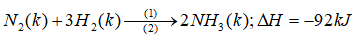
Theo nguyên lí dịch chuyển cân bằng Lechatelier
a) Khi tăng nhiệt độ cân bằng hóa học dịch chuyển theo chiều thu nhiệt, tức chiều nghịch, chiều phân hủy \(N{H_3}\)
b) Khi hóa lỏng \(N{H_3}\) nồng độ \(N{H_3}\) giảm cân bằng hóa học sẽ dịch chuyển theo chiều làm tăng nồng độ \(N{H_3}\) (chiều thuận) tạo thành \(N{H_3}\)
c) Giảm thể tích của hỗn hợp của phản ứng cân bằng hóa học dịch chuyển theo chiều làm giảm áp suất (chiều thuận) tạo ra \(N{H_3}\)
Câu 7 trang 48 SGK Hóa học 11 Nâng cao
Có thể phân biệt muối amoni với các muối khác bằng cách cho nó tác dụng với dung dịch kiềm, vì khi đó:
A. thoát ra một chất khí màu lục nhạt
B. thoát ra một chất khí không màu, mùi khai, làm xanh giấy quỳ tím ẩm
C. thoát ra một chất khí màu nâu đỏ, làm xamnh giấy quỳ tím ẩm.
D. thoát ra chất khí không màu, không mùi.
Giải
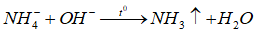
Chọn đáp án B
Câu 8* trang 48 SGK Hóa học 11 Nâng cao
Người ta có thể sản xuất amoniac để điều chế ure bằng cách chuyển hóa có xúc tác một hỗn hợp không khí, hơi nước và khí metan (thành phần chính của khí thiên nhiên).
Phản ứng điều chế \({H_2}\) và \(C{O_2}\) : \(C{H_4} + 2{H_2}O \to C{O_2} + 4{H_2}\) (1)
Phản ứng thu \({N_2}\) (từ không khí) và \(C{O_2}\): \(C{H_4} + 2{O_2} \to C{O_2} + 2{H_2}O\) (2)
Phản ứng tổng hợp \(N{H_3}\) :
![]()
Để sản xuất khí amoniac, nếu lấy 841,7 \({m^3}\)không khí (chứa 21,03% \({O_2}\), 78,02 \({N_2}\), còn lại là khí hiếm), thì cần phải lấy bao nhiêu \({m^3}\) khí metan và bao nhiêu \({m^3}\) hơi nước để có đủ lượng \({N_2}\) và \({H_2}\) theo tỉ lệ 1:3 về thể tích dùng cho phản ứng tổng hợp amoniac. Giả thiết các phản ứng (1) và (2) đều xảy ra hoàn thành và các thể tích khi được đo ở cùng điều kiện.
Giải
Thể tích khí \({O_2}\) và khí \({N_2}\) trong 841,7 \({m^3}\) không khí:
\({V_{{O_2}}} = \frac{{841,7.21,03}}{{100}} = 177,01({m^3});\)
\({V_{{N_2}}} = \frac{{841,7.78,02}}{{100}} = 656,69({m^3})\)

\({V_{{H_2}}}\)cần = \(3.{V_{{N_2}}} = 3.656,69 = 1970,08({m^3})\)
Từ phương trình (1): \(C{H_4} + 2{H_2}O \to C{O_2} + 4{H_2}\)
\(1{m^3} \to 2{m^3} \to 1{m^3} \to 4{m^3}\)
? \( \leftarrow \) ? \( \leftarrow \) 1970,08 \({m^3}\)
\({V_{C{H_4}}} = \frac{{1970,08}}{4} = 492,52({m^3})\)
\({V_{{H_2}O}} = 2.492,52 = 985,04({m^3})\)
Từ phương trình (2): \(C{H_4} + 2{O_2} \to C{O_2} + 2{H_2}O\)
\(1{m^3} \to 2{m^3}\)
? \( \leftarrow \)177,01 \({m^3}\) \( \to \) 177,01 \({m^3}\)
\({V_{C{H_4}}} = \frac{{177,01}}{2} = 88,5({m^3})\)
Vậy thể tích \(C{H_4}\) và \({H_2}\) tổng cộng cần:
\({V_{C{H_4}}} = 492,52 + 88m5 = 581,02({m^3});\)
\({V_{{H_2}O}} = 985,04 - 177,01 = 808,03({m^3})\)
Giaiaitap.me
Giải bài tập trang 55 bài 12 axit nitric và muối nitrat SGK Hóa học 11 Nâng cao. Câu 1: Viết công thức electron và công thức cấu tạo axit nitic và cho biết nguyên tố nitơ có số oxi hóa là bao nhiêu...
Giải bài tập trang 55 bài 12 axit nitric và muối nitrat SGK Hóa học 11 Nâng cao. Câu 5: Tại sao khi điều chế axit nitric bốc khói phải sử dụng...
Giải bài tập trang 57 bài 13 luyện tập tính chất của nito và hợp chất của nito SGK Hóa học 11 Nâng cao. Câu 1: Viết các phương trình hóa học để thực hiện các sơ đồ chuyển hóa sau...
Giải bài tập trang 62 bài 14 photpho SGK Hóa học 11 Nâng cao. Câu 1: Tại sao photpho đỏ và photpho trắng lại khác nhau về tính chất vật lí ? Trong điều kiện nào thì photpho trắng chuyển thành photpho đỏ và ngược lại?...
