Bài tập trắc nghiệm 4.18 trang 30 sách bài tập(SBT) hóa học 11
4.18. Trong số 9 chất dưới đây, những chất nào là đồng đẳng của nhau ? Những chất nào là đồng phân của nhau ?
1. \(C{H_3}C{H_2}C{H_3}\)
2. \(C{H_3}C{H_2}C{H_2}Cl\)
3. \(C{H_3}C{H_2}C{H_2}C{H_3}\)
4. \(C{H_3}CHClC{H_3}\)
5. \({(C{H_3})_2}CHC{H_3}\)
6. \(C{H_3}C{H_2}CH = C{H_2}\)
7. \(C{H_3}CH = C{H_2}\)
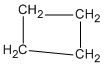
8. 
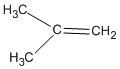
9. 
Hướng dẫn trả lời:
Các chất đồng đẳng :
(1) và (3) ; (1) và (5) ; (6) và (7) ; (7) và (9).
Bài tập 4.19 Trang 30 sách bài tập (SBT) Hóa Học 11
4.19. Hỗn hợp khí A chứa hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Lấy 1,12 lít A (đktc) đem đốt cháy hoàn toàn. Sản phẩm cháy được dẫn qua bình (1) đựng H2S04 đặc, sau đó qua bình (2) đựng dung dịch NaOH (có dư). Sau thí nghiệm, khối lượng bình (1) tăng 2,16 g và bình (2) tăng 7,48 g. Hãy xác định công thức phân tử và phần trăm về thể tích của từng chất trong hỗn hợp A.
Hướng dẫn trả lời:
Cách 1. Hai hiđrocacbon kế tiếp nhau trong dãy đồng đẳng có công thức phân tử là CxHy và Cx+1Hy+2.
Đặt công thức chung của hai chất đó là \({C_{\overline x }}{H_{\overline y }}\) trong đó \(\overline x \) là số nguyên tử cacbon trung bình (x < \(\overline x \) < x +1) và \(\overline y \) là số nguyên tử hiđro trung bình (y < \(\overline y \) < y + 2).
\({C_{\overline x }}{H_{\overline y }}\) + (\(\overline x \) + \(\frac{{\overline y }}{4}\))\({O_2}\) \( \to \) \(\overline x \)\(C{O_2}\) + \(\frac{{\overline y }}{2}\)\({H_2}O\)
n\({H_2}O\) + \({H_2}S{O_4}\) \( \to \) \({H_2}S{O_4}\).n\({H_2}O\)
\(C{O_2}\) + 2\(NaOH\) \( \to \) \(N{a_2}C{O_3}\) + \({H_2}O\)
Số mol 2 chất mang đốt : \(\frac{{1,12}}{{22,4}}\) = 0,0500 (mol).
Số mol \({H_2}O\) : \(\frac{{2,16}}{{18}}\) = 0,120 (mol).
Số mol CO2: \(\frac{{7,48}}{{44}}\) = 0,170(mol).
Theo phương trình : 1 mol \({C_{\overline x }}{H_{\overline y }}\) tạo ra \(\overline x \) mol CO2 và \(\overline y \) mol \({H_2}O\).
Theo đầu bài: 0,0500 mol \({C_{\overline x }}{H_{\overline y }}\) tạo ra 0,170 mol CO2 và 0,120 mol \({H_2}O\).
\(\overline {\overline x } \) = \(\frac{{0,17}}{{0,05}}\) = 3,4 ; x < 3,4 < x + 1 \( \Rightarrow \) 2,4 < x < 3,4
x là số nguyên nên x = 3
\(\frac{{\overline y }}{2}\) = \(\frac{{0,12}}{{0,05}}\) = 2,4 \( \Rightarrow \) \(\overline y \) = 4,8 \( \to \) y < 4,8 < y + 2
\( \Rightarrow \) 2,80 < y < 4,80.
Trong khoảng này có hai số nguyên là 3 và 4 nhưng số nguyên tử hiđro trong một phân tử hiđrocacbon không bao giờ là số lẻ nên y = 4.
Công thức phân tử của hai chất là \({C_3}{H_4}\) và \({C_4}{H_6}\). Đặt lượng \({C_3}{H_4}\) là a mol, lượng \({C_4}{H_6}\) là b mol:
\(\left\{ \begin{array}{l}
a + b = 0,05\\
3a + 4b = 0,17
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
a = 0,03\\
b = 0,02
\end{array} \right.\)
% về thể tích (cũng là % về số mol) của \({C_3}{H_4}\) trong hỗn hợp A :
\(\frac{{0,03}}{{0,05}}\).100% = 60,0%.
% về thể tích của \({C_4}{H_6}\) trong hỗn hợp A là 40,0%.
Cách 2 : Đặt lượng CxHy là a mol, lượng Cx+1Hy+2 là b mol.
Ta có : a + b = 0,05 (1)
\({C_x}{H_y} + (x + \frac{y}{4}){O_2} \to xC{O_2} + \frac{y}{2}{H_2}O\)
a mol ax mol \(\frac{{ay}}{2}\) mol
\({C_{x + 1}}{H_{y + 2}} + (x + \frac{y}{4} + 1,5){O_2} \to (x + 1)C{O_2} + \frac{{y + 2}}{2}{H_2}O\)
b mol b.(x+1) mol \(\frac{{b(y + 2)}}{2}\)
Số mol \(C{O_2}\) : ax + b(x + 1) = 0,170 (2)
Số mol \({H_2}O\) : \(\frac{{ay + b(y + 2)}}{2} = 0,12\) (3)
Từ (2) ta có (a + b)x + b = 0,170 ;
b = 0,170-0,0500x
b là số mol của một trong hai chất nên 0 < b < 0,0500.
Do đó 0 < 0,170 - 0,0500x < 0,0500 \( \Rightarrow \) 2,40 < X < 3,40 \( \Rightarrow \) X = 3.
\( \Rightarrow \) b = 0,1700 - 0,0500 X 3 = 0,0200 \( \Rightarrow \) a = 0,0500 - 0,0200 = 0,0300 Thay giá trị của a và b vào (3) ta có :
0,03y + 0,02(y + 2) = 0 \( \Rightarrow \) y = 4.
Trả lời : \({C_3}{H_4}\) chiếm 60,0% thể tích hỗn hợp A.
\({C_4}{H_6}\) chiếm 40,0% thể tích hỗn hợp A.
Bài tập 4.20 trang 30 sách bài tập(SBT) hóa học 11
4.19. Hỗn hợp M chứa ba hiđrocacbon là đồng phân của nhau. Khi đốt cháy hoàn toàn 1,80 g M, thu được 2,80 lít C02 (đktc).
1. Xác định công thức phân tử của các chất mang đốt biết rằng tỉ khối hơi của M đối với oxi là 2,25.
2. Dựa vào thuyết cấu tạo hoá học, hãy viết công thức cấu tạo khai triển và công thức cấu tạo rút gọn của từng chất trong hỗn hợp M.
Hướng dẫn trả lời:
Các chất đồng phân có cùng CTPT và có PTK bằng nhau. Các chất trong hỗn hợp M đều là \({C_{\rm{x}}}{H_y}\).
Khối lượng C trong 2,8 lít CO2: \(\frac{{12.2,8}}{{22,4}}\) = 1.50(g).
Đó cũng là khối lượng C trong 1,80 g \({C_{\rm{x}}}{H_y}\) , vậy khối lượng H : 1,80- 1,50 = 0,30 (g).
x : y= \(\frac{{1,5}}{{12}}:\frac{{0,3}}{1}\) = 0,125 : 0,30 = 5:12.
Công thức đơn giản nhất là \({C_5}{H_{12}}\).
Khối lượng 1 mol \({C_{\rm{x}}}{H_y}\) : 2,25 X 32,0 = 72,0 (g).
Do đó, công thức phân tử cũng là \({C_5}{H_{12}}\).
Công thức cấu tạo của các đồng phân :
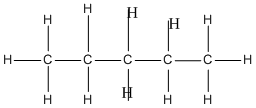 hay \(C{H_3} - C{H_2} - C{H_2} - C{H_2} - C{H_3}\)
hay \(C{H_3} - C{H_2} - C{H_2} - C{H_2} - C{H_3}\)
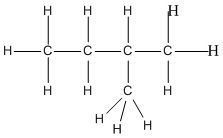 hay
hay 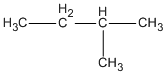
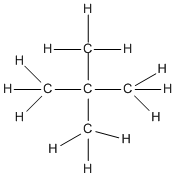 hay
hay 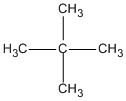
Bài tập 4.21 trang 30 sách bài tập(SBT) hóa học 11
4.21. Hỗn hợp M ở thể lỏng, chứa hai hợp chất hữu cơ kế tiếp nhau trong một dãy đồng đẳng. Nếu làm bay hơi 2,58 g M thì thể tích hơi thu được đúng bằng thể tích của 1,40 g khí N2 ở cùng điều kiện. Đốt cháy hoàn toàn 6,45 g M thì thu được 7,65 g H20 và 6,72 lít C02 (đktc).
Xác định công thức phân tử và phần trăm khối lượng của từng chất trong hỗn hợp M.
Hướng dẫn trả lời:
Số mol 2 chất trong 2,58 g M : \(\frac{{1,4}}{{28}}\) = 0,05 (mol).
Số mol 2 chất trong 6,45 g M : \(\frac{{0,05.6,45}}{{2,58}}\) = 0,125 (mol).
Khi đốt hỗn hợp M, thu được CO2 và H20 ; vậy các chất trong hỗn hợp phải chứa C và H, có thể có O. Hai chất lại kế tiếp nhau trong một dãy đồng đẳng (nghĩa là hom nhau 1 nhóm CH2) nên công thức phân tử hai chất đó là CxHyOz và Cx+1Hy+2Oz (x, y nguyên và > 0 ; z nguyên và > 0).
Giả sử trong 6,45 g M có a moi CxHyOz và b mol Cx+1 Hy+2Oz:
\(\left\{ \begin{array}{l}
a + b = 0,125(1)\\
(12{\rm{x}} + y + 16{\rm{z}})a + (12{\rm{x}} + y + 16{\rm{z}} + 14)b = 6,45(2)
\end{array} \right.\)
\({C_{\rm{x}}}{H_y}{O_{\rm{z}}} + (x + \frac{y}{4} - \frac{z}{2}){O_2} \to xC{O_2} + \frac{y}{2}{H_2}O\)
a mol xa mol \(\frac{{ya}}{2}\) mol
\({C_{{\rm{x + 1}}}}{H_{y + 2}}{O_{\rm{z}}} + (x + \frac{y}{4} - \frac{z}{2} + 1,5){O_2} \to (x + 1)C{O_2} + \frac{{y + 2}}{2}{H_2}O\)
b mol (x+1)b mol \(\frac{{(y + 2)b}}{2}\)
Số mol CO2: xa + (x + l)b = \(\frac{{6,72}}{{22,4}}\) = 0,3 (mol) (3)
Số mol \({H_2}O\): \(\frac{{y{\rm{a + }}(y + 2)b}}{2} = \frac{{7,65}}{{18}}\) = 0,425 (mol)
\( \Rightarrow \) ya + (y + 2)b = 0,85 (4)
Giải hệ phương trình :
Biến đổi (3) ta có x(a + b) + b = 0,300
b = 0,300-0,125x
0 < b < 0,125 \( \Rightarrow \) 0 < 0,300 - 0,125x < 0,125
1,40 < x < 2,40
\( \Rightarrow \) x = 2 ; b = 0,300 - 0,125.2 = 0,05.
\( \Rightarrow \) a = 0,125 - 0,05 = 0,075.
Thay giá trị của a và b vào (4) ta có :
0,0750y + 0,0500(y + 2) = 0,85
\( \Rightarrow \) y = 6.
Thay giá trị của a, b, x, y vào (2) ta tìm được z = 1.
Thành phần hỗn hợp M :
Khối lượng C2H6O chiếm \(\frac{{0,075.46}}{{6.45}}\). 100% = 53,5%.
Khối lượngC3HgO chiếm \(\frac{{0,05.60}}{{6.45}}\). 100% = 46,5%.
Bài tập 4.22 trang 30 sách bài tập(SBT) hóa học 11
4.22. Hỗn hợp X chứa ba chất hữụ cơ đồng phân. Nếu làm bay hơi 2,10 g X thì thể tích hơi thu được bằng thể tích của 1,54 g khí C02 ở cùng điều kiện. Để đốt cháy hoàn toàn 1,50 g X cần dùng vừa hết 2,52 lít 02 (đktc). Sản phẩm cháy chỉ có C02 và H20 theo tỉ lệ 11 : 6 về khối lượng.
1. Xác định công thức phân tử của ba chất trong X.
2. Dựa vào thuyết cấu tạo hoá học, hãy viết công thức cấu tạo (triển khai và rút gọn) của từng chất đó.
Hướng dẫn trả lời:
Ba chất đồng phân có công thức phân tử giống nhau. Đốt X ta chỉ được C02 và H20, vậy các chất trong X có chứa C, H và có thể có chứa O.
Theo định luật bảo toàn khối lượng :
\({m_{C{O_2}}} + {m_{{H_2}O}} = {m_X} + {m_{{O_2}}} = 1,5 + \frac{{2,52}}{{22,4}}.32 = 5,1(g)\)
Mặt khác \({m_{C{O_2}}}:{m_{{H_2}O}}\) =11:6
Từ đó tìm được : \({m_{C{O_2}}}\) = 3,30 g và \({m_{{H_2}O}}\) = 1,80 g
Khối lượng C trong 3,30 g C02: \(\frac{{12.3,3}}{{44}}\) = 0,9 (g).
Khối lương H trong 1,80 g H20 : \(\frac{{2.1,8}}{{18}}\) =0,2 (g)
Khối lượng o trong 1,50 g X : 1,50 - 0,9 - 0,2 = 0,4 (g).
Các chất trong X có dạng CxHyOz
x : y : z = \(\frac{{0,9}}{{12}}:\frac{{0,2}}{1}:\frac{{0,4}}{{16}}\) = 0,075 : 0,2 : 0,025 = 3:8:1.
Công thức đơn giản nhất là \({C_3}{H_8}O\).
\({M_{\rm{x}}} = \frac{{2,1.44}}{{1,54}} = 60(g/mol) \Rightarrow \) CTPT cũng là \({C_3}{H_8}O\).
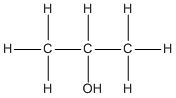
Các CTCT:
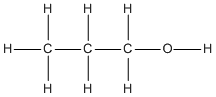 ; \(C{H_3} - C{H_2} - C{H_2} - OH\)
; \(C{H_3} - C{H_2} - C{H_2} - OH\)
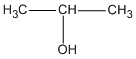
 ;
; 
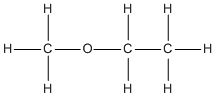 ; \(C{H_3} - O - C{H_2} - C{H_3}\)
; \(C{H_3} - O - C{H_2} - C{H_3}\)
Giaibaitap.me
Giải bài tập trang 31 bài 23 phản ứng hữu cơ Sách bài tập (SBT) hóa học 11. Câu 4.23: Phản ứng sau thuộc loại phản ứng gì ?...
Giải bài tập trang 32 bài 24 luyện tập hợp chất hữu cơ, công thức phân tử và công thức cấu tạo Sách bài tập (SBT) hóa học 11. Câu 4.29: Cho dãy chất : CH4 ; C6H6 ; C6H5-OH ; C2H5ZnI ; C2H5PH2. Nhận xét nào đưới đây đúng ?...
Giải bài tập trang 32 bài 23 phản ứng hữu cơ Sách bài tập (SBT) hóa học 11. Câu 4.28: Hãy sắp xếp mỗi phản ứng dưới đây vào loại phản ứng thích hợp (phản ứng thế, phản ứng tách, phản ứng cộng)...
Giải bài tậpp trang 33, 34 bài 24 luyện tập hợp chất hữu cơ, công thức phân tử và công thức cấu tạo Sách bài tập hóa học 11. Câu 4.33: Trong số các chất hữu cơ đã được học ở lớp 9, hãy kể ra 2 cặp chất có công thức phân tử khác nhau nhưng có cùng công thức đơn giản nhất...
